Nat Med | Жоон ичегинин рагынын шишик, иммундук жана микробдук ландшафтын интеграцияланган картага түшүрүү үчүн мультиомика ыкмасы микробиомдун иммундук система менен өз ара аракеттенишин ачып берет.
Акыркы жылдары жоон ичеги рагынын биомаркерлери кеңири изилденгени менен, учурдагы клиникалык көрсөтмөлөр дарылоо боюнча сунуштарды аныктоо үчүн шишик-лимфа түйүнү-метастаз стадиясына жана ДНКнын дал келбестигинин калыбына келүүсүнүн (MMR) кемчиликтерин же микросателлиттин туруксуздугун (MSI) аныктоого (стандарттык патологиялык тестирлөөдөн тышкары) гана таянат. Изилдөөчүлөр Рак геномунун атласынын (TCGA) жоон ичеги рагынын когортасындагы ген экспрессиясына негизделген иммундук реакциялар, микробдук профилдер жана шишик стромасы менен бейтаптардын жашоо деңгээлинин ортосундагы байланыштын жоктугун белгилешти.
Изилдөөлөр өнүккөн сайын, рактын клеткалык, иммундук, стромалдык же микробдук мүнөзүн кошо алганда, баштапкы жоон ичеги рагынын сандык мүнөздөмөлөрү клиникалык натыйжалар менен олуттуу байланышта экени кабарланган, бирок алардын өз ара аракеттенүүсү бейтаптардын натыйжаларына кандай таасир этери жөнүндө түшүнүк дагы эле чектелүү.
Фенотиптик татаалдык менен натыйжанын ортосундагы байланышты талдоо үчүн Катардагы Сидра медициналык изилдөө институтунун изилдөөчүлөрүнүн тобу жакында эле микробиомдун мүнөздөмөлөрүн жана иммундук баш тартуу константаларын (ICR) айкалыштыруу аркылуу жакшы жашоо көрсөткүчтөрү бар бейтаптардын тобун аныктоочу интеграцияланган баллды (mICRoScore) иштеп чыгып, текшеришти. Топ баштапкы жоон ичегинин рагы менен ооруган 348 бейтаптын жаңы тоңдурулган үлгүлөрүнө комплекстүү геномдук анализ жүргүздү, анын ичинде шишиктердин жана дал келген дени сак жоон ичегинин тканынын РНК секвенирлөөсү, бүтүндөй экзом секвенирлөөсү, терең Т-клетка рецептору жана 16S бактериялык рРНК ген секвенирлөөсү, микробиомду андан ары мүнөздөө үчүн бүтүндөй шишик геномунун секвенирлөөсү менен толукталды. Изилдөө Nature Medicine журналында "Жоон ичегинин рагынын интеграцияланган шишик, иммундук жана микробиомдук атласы" деп жарыяланган.

Nature Medicine журналында жарыяланган макала
AC-ICAMга сереп
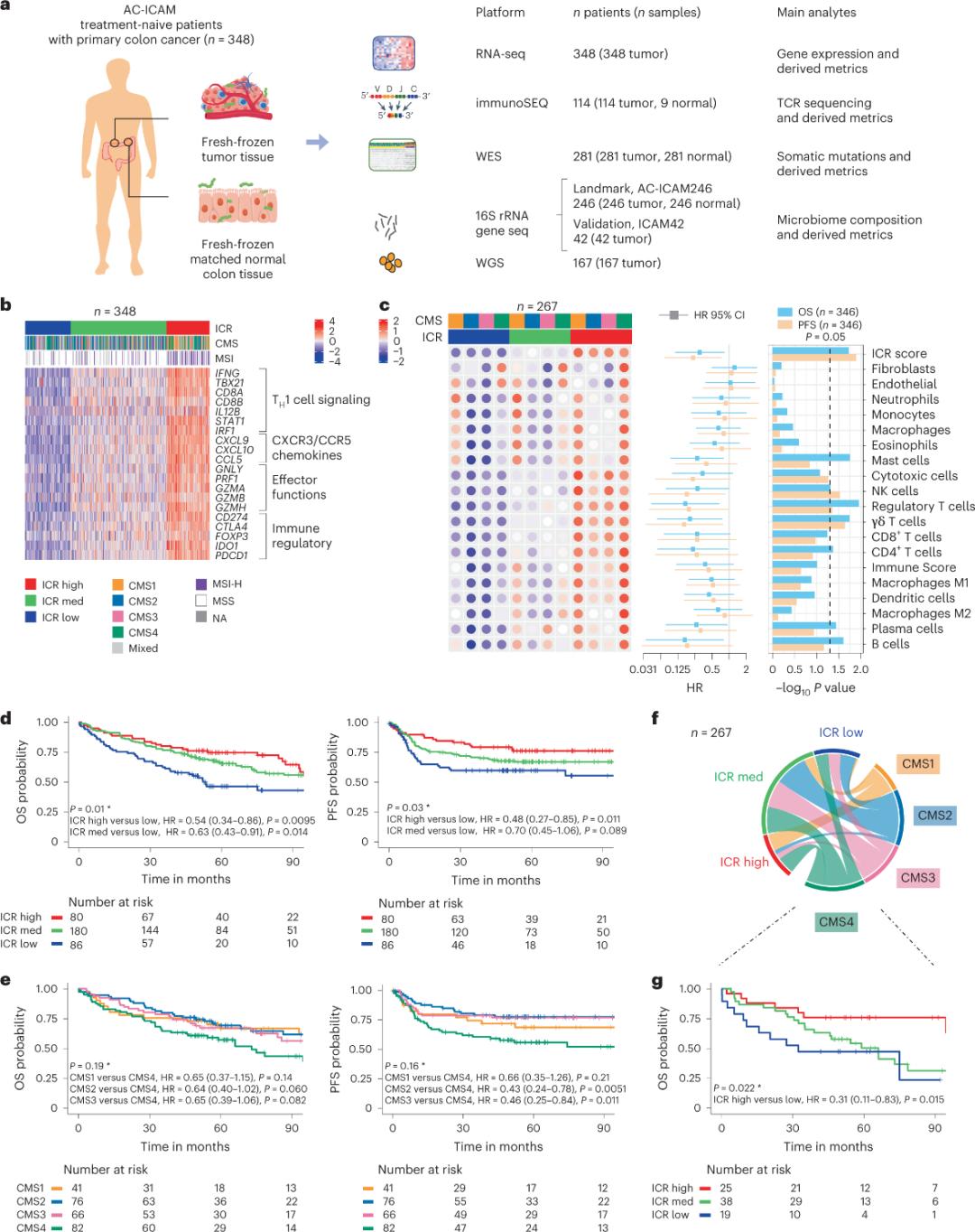
Изилдөөчүлөр системалуу терапиясыз жоон ичеги рагынын гистологиялык диагнозу коюлган бейтаптардан жаңы тоңдурулган шишик үлгүлөрүн жана дал келген жанаша жайгашкан дени сак жоон ичеги ткандарын (шишик-нормалдуу жуптарды) талдоо үчүн ортогоналдык геномдук платформаны колдонушкан. Толук экзомдук секвенирлөөгө (WES), РНК-секвенирдик маалыматтардын сапатын көзөмөлдөөгө жана инклюзия критерийлерин скринингге негизделген 348 бейтаптын геномдук маалыматтары сакталып, орточо байкоо жүргүзүү убактысы 4,6 жыл болгон кийинки анализ үчүн колдонулган. Изилдөө тобу бул ресурсту Sidra-LUMC AC-ICAM: Иммундук-рак-микробиомдук өз ара аракеттенүү картасы жана колдонмосу деп атады (1-сүрөт).
ICRди колдонуу менен молекулярдык классификациялоо
Изилдөө тобу рактын үзгүлтүксүз иммундук көзөмөлү үчүн иммундук генетикалык маркерлердин модулдук топтомун, башкача айтканда, четке кагуунун иммундук константасын (ICR) кармап, ICRди меланома, табарсык рагы жана эмчек рагы сыяктуу ар кандай рак түрлөрүн камтыган 20 гендик панелге бириктирүү менен оптималдаштырды. ICR ошондой эле эмчек рагын кошо алганда, ар кандай рак түрлөрүндөгү иммунотерапияга жооп берүү менен байланыштуу болгон.
Биринчиден, изилдөөчүлөр AC-ICAM когортасынын ICR кол тамгасын текшерип, когортаны үч кластерге/иммундук субтиптерге бөлүү үчүн ICR генине негизделген биргелешип классификациялоо ыкмасын колдонушту: жогорку ICR (ысык шишиктер), орточо ICR жана төмөнкү ICR (муздак шишиктер) (1b-сүрөт). Изилдөөчүлөр жоон ичеги рагынын транскриптомго негизделген классификациясы болгон консенсус молекулярдык субтиптери (CMS) менен байланышкан иммундук тенденцияны мүнөздөштү. CMS категорияларына CMS1/иммундук, CMS2/канондук, CMS3/метаболикалык жана CMS4/мезенхималык кирген. Анализ көрсөткөндөй, ICR упайлары бардык CMS субтиптериндеги айрым рак клеткаларынын жолдору менен терс корреляцияланган жана иммуносупрессивдүү жана стромалдык жолдор менен оң корреляциялар CMS4 шишиктеринде гана байкалган.
Бардык CMSтерде табигый киллер (NK) клеткаларынын жана Т клеткаларынын топтомдорунун көптүгү ICR жогорку иммундук топтомдорунда эң жогорку болгон, ал эми башка лейкоциттердин топтомдорунда чоң өзгөрмөлүүлүк байкалган (1c-сүрөт). ICR иммундук топтомдорунда ар кандай OS жана PFS болгон, ICR төмөнкүдөн жогоркуга чейин прогрессивдүү жогорулаган (1d-сүрөт), бул ICRдин жоон ичеги рагындагы прогностикалык ролун тастыктаган.
1-сүрөт. AC-ICAM изилдөөсүнүн дизайны, иммундук системага байланыштуу гендин кол тамгасы, иммундук жана молекулярдык түрчөлөрү жана жашоо узактыгы.
ICR шишик менен байытылган, клондук түрдө күчөтүлгөн Т клеткаларын кармайт
Шишик тканына инфильтрацияланган Т клеткаларынын аз гана бөлүгү шишик антигендерине спецификалык экени кабарланган (10% дан аз). Ошондуктан, шишик ичиндеги Т клеткаларынын көпчүлүгү байкоочу Т клеткалары (байкоочу Т клеткалары) деп аталат. Продуктивдүү TCRлери бар кадимки Т клеткаларынын саны менен эң күчтүү корреляция стромалдык клеткалардын жана лейкоциттердин субпопуляцияларында (РНК-секвенция менен аныкталган) байкалган, аны Т клеткаларынын субпопуляцияларын баалоо үчүн колдонсо болот (2a-сүрөт). ICR кластерлеринде (жалпы жана CMS классификациясы) иммундук SEQ TCRлеринин эң жогорку клондуулугу ICR-жогорку жана CMS субтибиндеги CMS1/иммундук топтордо байкалган (2c-сүрөт), ICR-жогорку шишиктердин эң жогорку үлүшү менен. Бүтүндөй транскриптомду (18 270 ген) колдонуу менен, алты ICR гени (IFNG, STAT1, IRF1, CCL5, GZMA жана CXCL10) TCR иммундук SEQ клондуулугу менен оң байланышкан алдыңкы он гендин катарына кирген (2d-сүрөт). ImmunoSEQ TCR клоналдыктыгы шишикке жооп берүүчү CD8+ маркерлерин колдонуу менен байкалган корреляцияларга караганда көпчүлүк ICR гендери менен күчтүүрөөк корреляцияланган (2f жана 2g-сүрөттөр). Жыйынтыктап айтканда, жогорудагы анализ ICR кол тамга шишик менен байытылган, клондук жактан күчөтүлгөн Т клеткаларынын бар экендигин чагылдырарын жана анын прогностикалык кесепеттерин түшүндүрүшү мүмкүн экенин көрсөтүп турат.
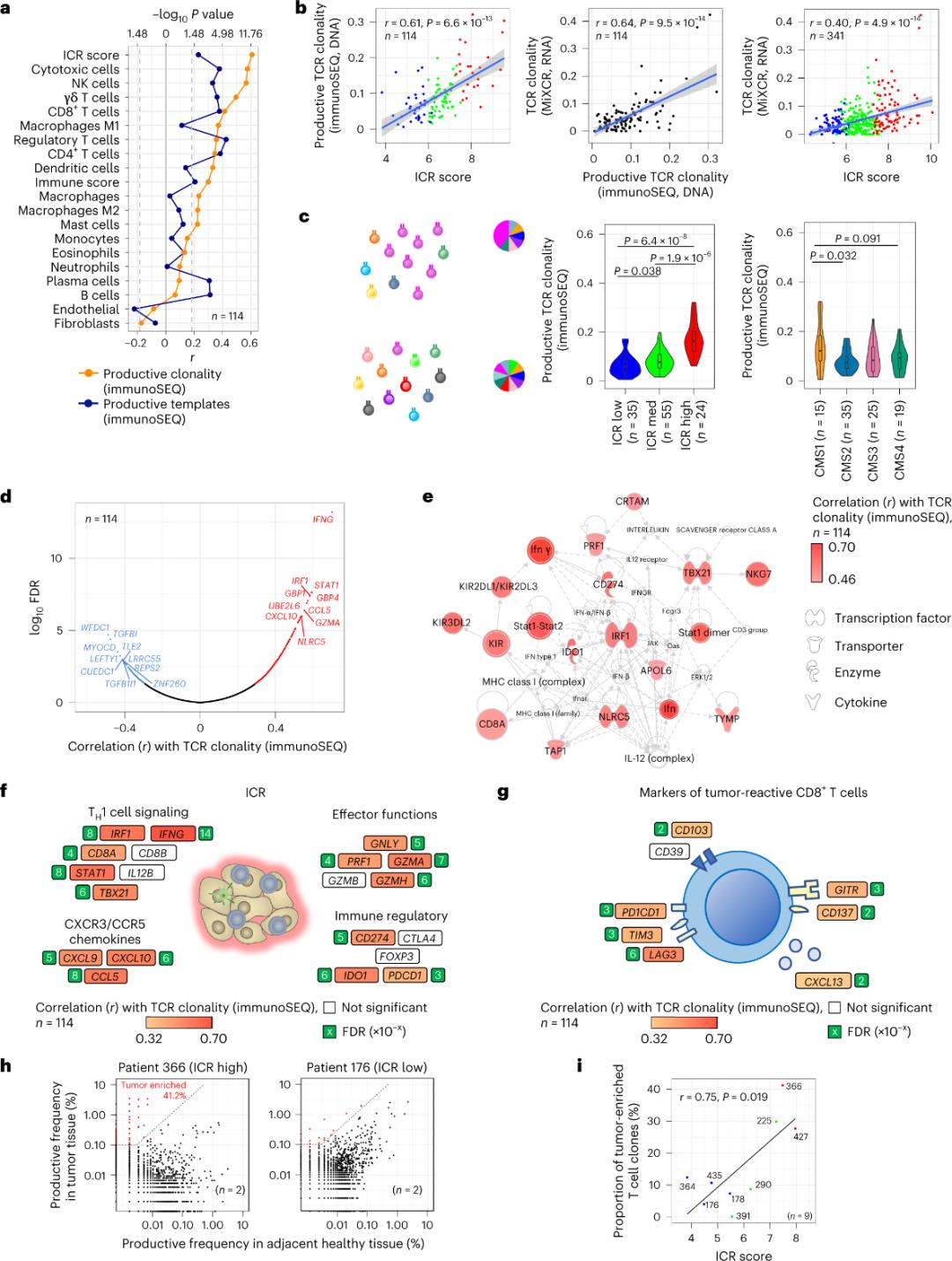
2-сүрөт. TCR көрсөткүчтөрү жана иммундук байланыштуу гендер, иммундук жана молекулярдык түрчөлөр менен корреляция.
Дени сак жана жоон ичеги рагынын ткандарындагы микробиомдун курамы
Изилдөөчүлөр 246 бейтаптын дал келген шишигинен жана дени сак жоон ичеги тканынан алынган ДНКны колдонуп, 16S рРНК секвенирлөөсүн жүргүзүшкөн (3a-сүрөт). Текшерүү үчүн изилдөөчүлөр кошумча түрдө анализ үчүн жеткиликтүү болгон дал келген кадимки ДНКсы жок кошумча 42 шишик үлгүсүнөн алынган 16S рРНК ген секвенирлөө маалыматтарын талдашкан. Алгач, изилдөөчүлөр дал келген шишиктер менен дени сак жоон ичеги тканынын ортосундагы флоранын салыштырмалуу көптүгүн салыштырышкан. Clostridium perfringens дени сак үлгүлөргө салыштырмалуу шишиктерде бир кыйла көбөйгөн (3a-3d-сүрөт). Шишик менен дени сак үлгүлөрдүн ортосунда альфа ар түрдүүлүгүндө (бир үлгүдөгү түрлөрдүн ар түрдүүлүгү жана көптүгү) олуттуу айырмачылыктар болгон эмес, ал эми ICR-төмөн шишиктерге салыштырмалуу ICR-жогорку шишиктерде микробдук ар түрдүүлүктүн бир аз төмөндөшү байкалган.
Микробдук профилдер менен клиникалык натыйжалардын ортосундагы клиникалык жактан маанилүү байланыштарды аныктоо үчүн изилдөөчүлөр 16S рРНК генинин секвенирлөө маалыматтарын колдонуп, жашоону алдын ала айткан микробиомдун өзгөчөлүктөрүн аныктоону көздөшкөн. AC-ICAM246да изилдөөчүлөр MBR классификаторлору деп аталган нөл эмес коэффициенттери бар (өлүмдүн дифференциалдык тобокелдиги менен байланышкан) 41 өзгөчөлүктү тандап алган OS Cox регрессия моделин иштетишкен (3f-сүрөт).
Бул окутуу когортасында (ICAM246) MBRдин төмөн упайы (MBR<0, MBRдин төмөндүгү) өлүм коркунучунун бир кыйла төмөндүгү менен байланышкан (85%). Изилдөөчүлөр эки көз карандысыз текшерилген когортада (ICAM42 жана TCGA-COAD) төмөн MBR (тобокелдик) менен узакка созулган OS ортосундагы байланышты тастыкташкан. (3-сүрөт) Изилдөө эндогастралдык кокк менен MBR упайларынын ортосунда күчтүү корреляцияны көрсөттү, алар шишик жана дени сак жоон ичеги ткандарында окшош болгон.
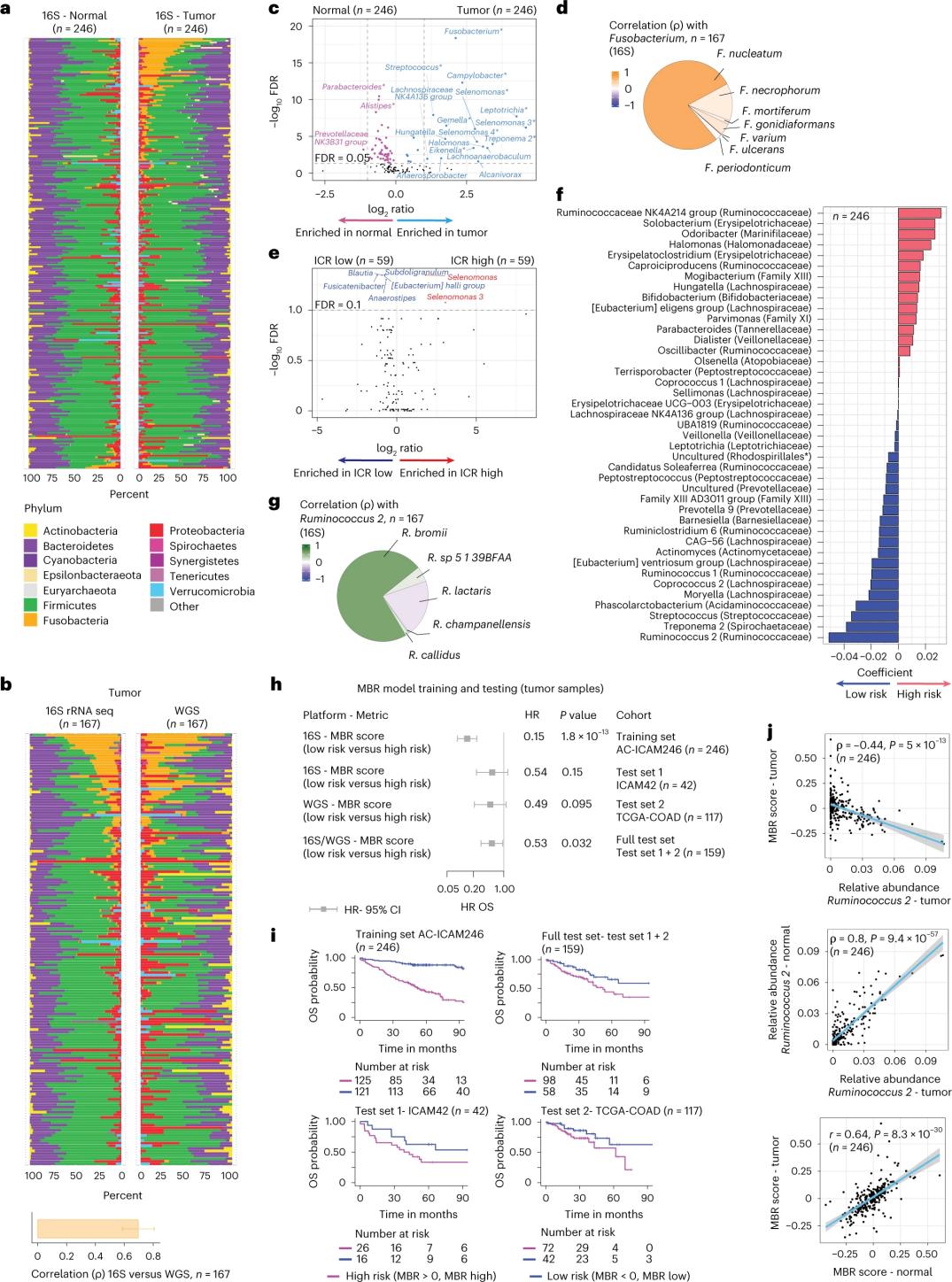
3-сүрөт. Шишиктеги жана дени сак ткандардагы микробиом жана ICR менен бейтаптын жашоосу ортосундагы байланыш.
Жыйынтык
Бул изилдөөдө колдонулган мультиомика ыкмасы жоон ичеги рагындагы иммундук жооптун молекулярдык белгисин кылдат аныктоого жана талдоого мүмкүндүк берет жана микробиом менен иммундук системанын ортосундагы өз ара аракеттенүүнү ачып берет. Шишиктин жана дени сак ткандардын терең TCR секвенирлөөсү ICRдин прогностикалык таасири анын шишикке бай жана, балким, шишик антигенине мүнөздүү Т-клетка клондорун кармоо жөндөмүнө байланыштуу болушу мүмкүн экенин көрсөттү.
AC-ICAM үлгүлөрүндөгү 16S рРНК генинин ырааттуулугун колдонуу менен шишик микробиомунун курамын талдоо менен, топ күчтүү прогностикалык мааниге ээ болгон микробиомдун кол тамгасын (MBR тобокелдик баллы) аныктады. Бул кол тамга шишик үлгүлөрүнөн алынганы менен, дени сак жоон ичегинин жана шишиктин MBR тобокелдик баллынын ортосунда күчтүү корреляция болгон, бул кол тамга бейтаптардын ичеги микробиомунун курамын чагылдырышы мүмкүн экенин көрсөтүп турат. ICR жана MBR баллдарын айкалыштыруу менен жоон ичеги рагы менен ооругандардын жашоо деңгээлин алдын ала айткан көп омикалык студенттик биомаркерди аныктоого жана текшерүүгө мүмкүн болду. Изилдөөнүн көп омикалык маалыматтар топтому жоон ичеги рагы биологиясын жакшыраак түшүнүү жана жекелештирилген терапиялык ыкмаларды табууга жардам берүү үчүн ресурс берет.
Жарыяланган убактысы: 2023-жылдын 15-июну
 中文网站
中文网站