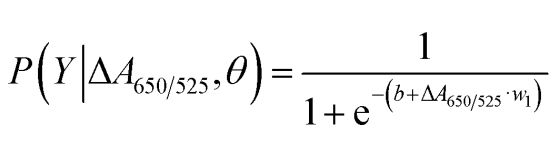Суюк биопсияга негизделген ракты эрте аныктоо - бул АКШнын Улуттук онкология институту тарабынан акыркы жылдары сунушталган ракты аныктоонун жана диагноз коюунун жаңы багыты, анын максаты - эрте ракты же ал тургай рак алдындагы жабыркоолорду аныктоо. Ал өпкө рагы, ашказан-ичеги шишиктери, глиома жана гинекологиялык шишиктер сыяктуу ар кандай залалдуу шишиктерди эрте аныктоо үчүн жаңы биомаркер катары кеңири колдонулуп келет.
Метилденген ландшафт (Methylscape) биомаркерлерин аныктоочу платформалардын пайда болушу ракты эрте аныктоону бир топ жакшыртууга жана бейтаптарды эң алгачкы дарылоо стадиясына жеткирүүгө мүмкүндүк берет.
Жакында эле изилдөөчүлөр цистеамин менен кооздолгон алтын нанобөлүкчөлөрүнө (Cyst/AuNPs) негизделген метилденүү ландшафтын аныктоо үчүн жөнөкөй жана түз сенсордук платформаны смартфонго негизделген биосенсор менен айкалыштырып иштеп чыгышты, ал ар кандай шишиктерди тез эрте скринингден өткөрүүгө мүмкүндүк берет. Лейкемияны эрте скрининг кан үлгүсүнөн ДНК алынгандан кийин 15 мүнөттүн ичинде, 90,0% тактык менен жүргүзүлүшү мүмкүн. Макаланын аталышы: Цистеамин менен капталган AuNPs жана машиналык окутууга негизделген смартфонду колдонуу менен адамдын канындагы рак ДНКсын тез аныктоо.
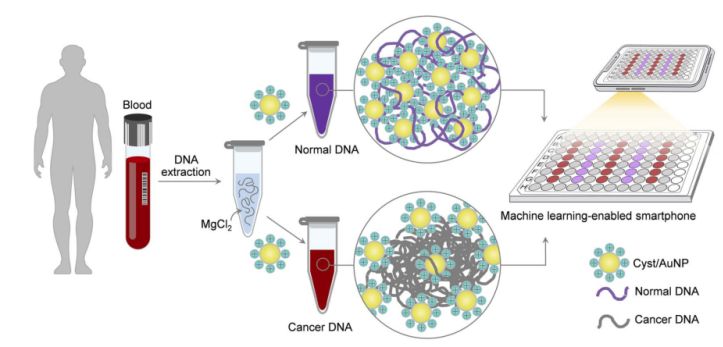
1-сүрөт. Cyst/AuNPs компоненттери аркылуу ракты скринингдөө үчүн жөнөкөй жана тез сенсордук платформаны эки жөнөкөй кадам менен ишке ашырууга болот.
Бул 1-сүрөттө көрсөтүлгөн. Алгач ДНК фрагменттерин эритүү үчүн суу эритмеси колдонулган. Андан кийин аралаш эритмеге киста/AuNP кошулган. Нормалдуу жана залалдуу ДНК ар кандай метилдөө касиеттерине ээ, натыйжада ДНК фрагменттери ар кандай өзүн-өзү чогултуу үлгүлөрүнө ээ. Нормалдуу ДНК бош агрегацияланат жана акырында киста/AuNP агрегацияланат, бул киста/AuNP кызылга жылган мүнөзгө алып келет, ошондуктан түстүн кызылдан кочкул кызылга өзгөрүшүн көз менен байкаса болот. Ал эми рак ДНКсынын уникалдуу метилдөө профили ДНК фрагменттеринин чоңураак кластерлеринин пайда болушуна алып келет.
96 кудуктан турган пластиналардын сүрөттөрү смартфондун камерасы аркылуу тартылган. Рактын ДНКсы спектроскопияга негизделген ыкмалар менен салыштырылып, машиналык окутуу менен жабдылган смартфон аркылуу өлчөнгөн.
Чыныгы кан үлгүлөрүндөгү ракты текшерүү
Сенсордук платформанын пайдалуулугун кеңейтүү үчүн, изилдөөчүлөр чыныгы кан үлгүлөрүндөгү кадимки жана рак ДНКсын ийгиликтүү айырмалаган сенсорду колдонушкан. CpG сайттарындагы метилдөө үлгүлөрү ген экспрессиясын эпигенетикалык жактан жөнгө салат. Дээрлик бардык рак түрлөрүндө ДНК метилдөөсүндөгү жана ошентип, шишиктин пайда болушуна өбөлгө түзгөн гендердин экспрессиясындагы өзгөрүүлөр кезектешип турганы байкалган.
ДНК метилдениши менен байланышкан башка рак ооруларынын модели катары изилдөөчүлөр лейкемия менен ооругандардын жана дени сак контролдоочулардын кан үлгүлөрүн колдонуп, лейкемия менен ооругандардын жана дени сак контролдоочулардын кан үлгүлөрүн колдонушкан. Бул метилдениш ландшафтынын биомаркери лейкемияны тез аныктоочу скрининг ыкмаларынан ашып түшпөстөн, бул жөнөкөй жана түшүнүктүү анализди колдонуу менен рактын кеңири түрүн эрте аныктоо мүмкүнчүлүгүн да көрсөтөт.
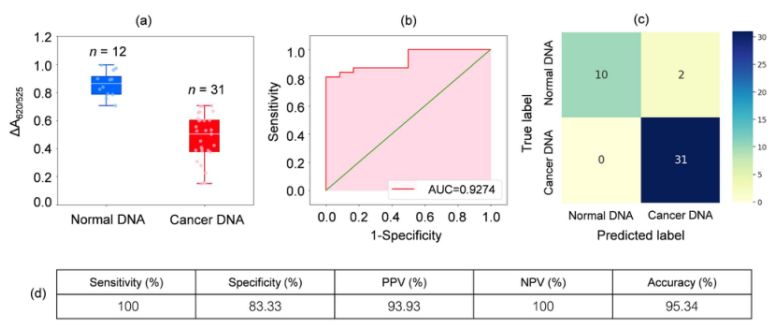
Лейкемия менен ооруган 31 бейтаптын жана 12 дени сак адамдын кан үлгүлөрүнөн алынган ДНК талданды. 2a-сүрөттөгү кутуча диаграммасында көрсөтүлгөндөй, рак үлгүлөрүнүн салыштырмалуу сиңирилиши (ΔA650/525) кадимки үлгүлөрдөгү ДНКга караганда төмөн болгон. Бул негизинен рак ДНКсынын тыгыз агрегациясына алып келген гидрофобдуктун жогорулашынан улам болгон, бул Киста/AuNP агрегациясынын алдын алган. Натыйжада, бул нанобөлүкчөлөр рак агрегаттарынын сырткы катмарларында толугу менен чачыранды болуп, кадимки жана рак ДНК агрегаттарына адсорбцияланган Киста/AuNP ар кандай дисперсияга алып келген. Андан кийин ROC ийри сызыктары босогону ΔA650/525 минималдуу маанисинен максималдуу мааниге чейин өзгөртүү менен түзүлгөн.
2-сүрөт.(а) Оптималдаштырылган шарттарда кадимки (көк) жана рак (кызыл) ДНКнын бар экендигин көрсөткөн киста/AuNP эритмелеринин салыштырмалуу абсорбциялык маанилери
(DA650/525) кутуча графиктеринин; (b) ROC анализи жана диагностикалык тесттерди баалоо. (c) Кадимки жана рак менен ооруган бейтаптарды диагноздоо үчүн башаламандык матрицасы. (d) Иштелип чыккан ыкманын сезгичтиги, спецификалуулугу, оң божомолдук мааниси (PPV), терс божомолдук мааниси (NPV) жана тактыгы.
2b-сүрөттө көрсөтүлгөндөй, иштелип чыккан сенсор үчүн алынган ROC ийри сызыгынын астындагы аянт (AUC = 0.9274) жогорку сезгичтикти жана өзгөчөлүктү көрсөттү. Кутуча диаграммасынан көрүнүп тургандай, кадимки ДНК тобун билдирген эң төмөнкү чекит рак ДНК тобун билдирген эң жогорку чекиттен жакшы бөлүнгөн эмес; ошондуктан, кадимки жана рак топторун айырмалоо үчүн логистикалык регрессия колдонулган. Көз карандысыз өзгөрмөлөрдүн жыйындысы берилгенде, ал рак же кадимки топ сыяктуу окуянын болуу ыктымалдыгын баалайт. Көз каранды өзгөрмө 0 жана 1 ортосунда өзгөрөт. Ошондуктан, натыйжада ыктымалдуулук пайда болот. Биз ракты аныктоо ыктымалдыгын (P) ΔA650/525 негизинде төмөнкүдөй аныктадык.
мында b=5.3533,w1=-6.965. Үлгүнү классификациялоо үчүн 0,5тен аз ыктымалдуулук кадимки үлгүнү, ал эми 0,5 же андан жогору ыктымалдуулук рак үлгүсүн көрсөтөт. 2c-сүрөттө классификациялоо ыкмасынын туруктуулугун текшерүү үчүн колдонулган кайчылаш текшерүүдөн келип чыккан башаламандык матрицасы көрсөтүлгөн. 2d-сүрөттө сезгичтикти, спецификалуулукту, оң божомолдоо маанисин (PPV) жана терс божомолдоо маанисин (NPV) камтыган методдун диагностикалык тесттик баалоосу кыскача баяндалган.
Смартфонго негизделген биосенсорлор
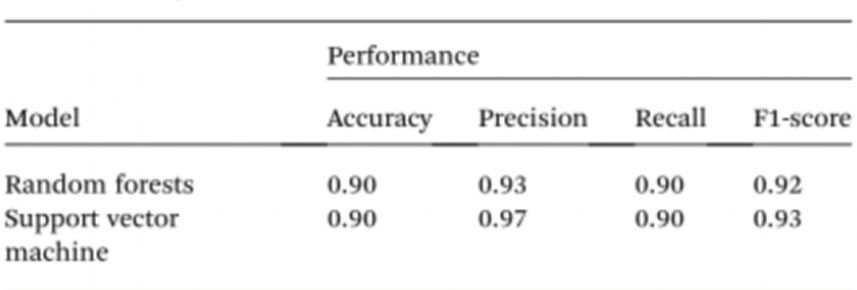
Спектрофотометрлерди колдонбостон үлгүлөрдү текшерүүнү андан ары жөнөкөйлөтүү үчүн, изилдөөчүлөр эритменин түсүн чечмелөө жана кадимки жана рак менен ооруган адамдарды айырмалоо үчүн жасалма интеллектти (ЖИ) колдонушкан. Муну эске алуу менен, уюлдук телефондун камерасы аркылуу тартылган 96 кудуктуу пластиналардын сүрөттөрүн колдонуу менен Cyst/AuNPs эритмесинин түсүн кадимки ДНКга (кызгылт көк) же рак менен ооруган ДНКга (кызыл) которуу үчүн компьютердик көрүү колдонулган. Жасалма интеллект нанобөлчөктөргө эритмелердин түсүн чечмелөөдө чыгымдарды азайтып, жеткиликтүүлүктү жакшырта алат жана смартфондун оптикалык жабдыктарын колдонбостон. Акырында, Random Forest (RF) жана Support Vector Machine (SVM) сыяктуу эки машиналык окутуу модели моделдерди курууга үйрөтүлдү. RF жана SVM моделдеринин экөө тең үлгүлөрдү 90,0% тактык менен оң жана терс деп туура классификациялашкан. Бул жасалма интеллектти мобилдик телефонго негизделген биосенсордо колдонуу толук мүмкүн экенин көрсөтүп турат.
3-сүрөт.(а) Сүрөт алуу этабы үчүн үлгүнү даярдоо учурунда жазылган эритменин максаттуу классы. (б) Сүрөт алуу этабында алынган сүрөттүн үлгүсү. (в) Сүрөттөн алынган 96-көзөнөктүү пластинанын ар бир көзөнөгүндөгү киста/AuNPs эритмесинин түсүнүн интенсивдүүлүгү (б).
Cyst/AuNP'терди колдонуу менен изилдөөчүлөр метилденүү ландшафтын аныктоо үчүн жөнөкөй сенсордук платформаны жана лейкемияны скринингдөө үчүн чыныгы кан үлгүлөрүн колдонууда кадимки ДНКны рак ДНКсынан айырмалай алган сенсорду ийгиликтүү иштеп чыгышты. Иштелип чыккан сенсор чыныгы кан үлгүлөрүнөн алынган ДНК лейкемия менен ооругандарда 15 мүнөттүн ичинде аз өлчөмдөгү рак ДНКсын (3nM) тез жана үнөмдүү түрдө аныктай алганын жана 95,3% тактыкты көрсөткөнүн көрсөттү. Спектрофотометрге болгон муктаждыкты жок кылуу менен үлгүлөрдү текшерүүнү андан ары жөнөкөйлөтүү үчүн, машиналык окутуу эритменин түсүн чечмелөө жана уюлдук телефондун сүрөтүн колдонуп, кадимки жана рак менен ооруган адамдарды айырмалоо үчүн колдонулган жана тактык 90,0%га жетишилген.
Шилтеме: DOI: 10.1039/d2ra05725e
Жарыяланган убактысы: 2023-жылдын 18-февралы
 中文网站
中文网站